每个异种移植模型的车载肿瘤的量化磷酸酪氨酸图谱显示了相似的信号,因此肿瘤之间具有良好的相关性,尽管存在一些异常值。例如,HCC827和H1975异种移植物有一个肿瘤表现出明显不同的信号传导,而H1975-hgf异种移植物表现出高度的同质性,而HCC827-er1相对于其他系则表现出更多的异质性。同样地,通过对每个已识别的含磷酪氨酸肽的量化值进行分级聚类,也证实了这些发现。单独或联合使用奥希替尼和JNJ-61186372对我们每个异种移植瘤模型的体内靶点疗效分析显示,在这个早期时间点,奥希替尼对肿瘤磷酸化酪氨酸的影响很强。
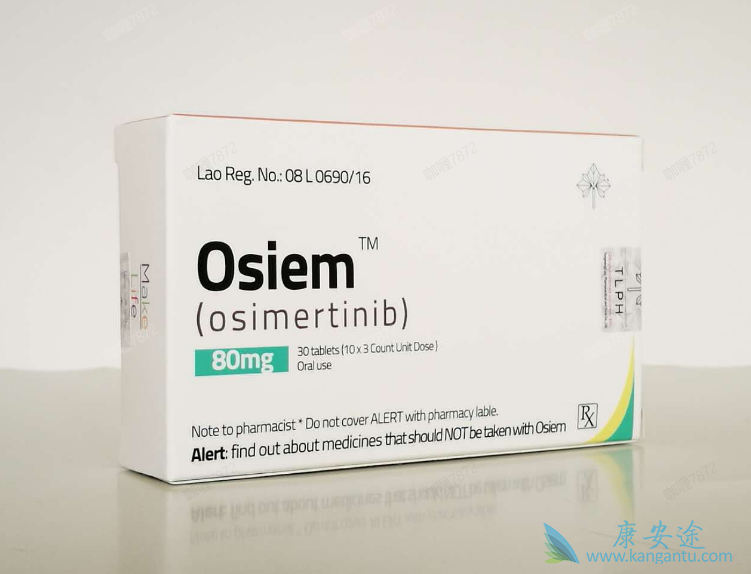
量化后的磷酸化酪氨酸图谱的相关性显示,与JNJ-61186372联合使用相比,使用奥希替尼治疗的所有肿瘤相关性更高,且都集中在一起。相比之下,单独使用JNJ-61186372治疗的肿瘤总体上表现出更大的肿瘤间异质性,并且与使用奥希替尼或奥希替尼与JNJ-61186372联合治疗的肿瘤相关性较差。
此外,定量磷酸化酪氨酸图谱的层次聚类显示了类似的趋势。确定体内目标这些疗法的功效,我们提取磷酸化水平的定量数据从表皮生长因子受体(Tyr1148和Tyr1173)选定的肽,遇到(Tyr1003,Tyr1295Tyr1365)和相关的近端适配器蛋白质Shc-transforming蛋白1(Shc1)(Tyr427)和Grb2-associated-binding蛋白1(Gab1)(Tyr659)。奥希替尼治疗的肿瘤显示EGFR、Shc1和Gab1的磷酸化水平显着下降,表明EGFR受到了强的靶向抑制。相比之下,在4种异种移植模型中,有3种模型对jnj-61186372治疗的肿瘤的总体趋势是只有非常适度的减少或无变化。此外,在JNJ-61186372治疗后Met扩增HCC827-ER1肿瘤中,Met磷酸化没有变化。综上所述,这些数据表明,与双特异性抗体相比,基于tki的治疗对EGFR信号传导抑制的作用更为迅速和显着。
确定了独特的肿瘤特异性重组耐药肿瘤
在长期使用奥希替尼或JNJ-61186372单药治疗期间,共有41个异种移植瘤产生耐药性并生长。总的来说,每个模型和治疗组肿瘤之间的磷酸酪氨酸图谱的相关性很强,表明在特定的治疗条件下,每个肿瘤可能都出现了共同的耐药反应。然而,分析也显示了显着的异质性,有1-3个肿瘤与剩下的JNJ-61186372-(H1975-HGF和HCC827-ER1)和奥希替尼治疗的肿瘤(HCC827-ER1)相关性较差。通过分级聚类,可以看到分析肿瘤中含磷酪氨酸肽水平的定量变化。
在这里,很明显,尽管肿瘤之间有良好的整体相关性,但每个单独的肿瘤都显示出独特的定量轮廓,因此,反映了肿瘤特异性信号通路的重新布线。此外,GO项富集分析证实了个体耐药肿瘤状态的独特性,考虑到磷脂肽之间的生物过程具有很大的多样性,且比例上调和下调。研究重点关注耐药肿瘤的上调过程,包括RTK和下游信号转导、创面愈合、基因表达调控、内吞作用和细胞粘附。有趣的是,考虑到RTKs在支持耐药肿瘤生长中所扮演的明确角色,我们惊讶于在每个治疗组中没有更统一的RTK信号上调。然而,尽管不是普遍的发现,某些肿瘤显示EGFR和/或ErbB家族成员或下游信号适配器酪氨酸残基磷酸化增加;最终,这些肿瘤可能通过上调erbb家族表达或erbb家族配体水平,或交叉激活EGFR家族的其他成员来适应,提示这些RTKs具有可塑性。另外,考虑到肿瘤内异质性的存在,这种治疗可能促进了已经具有观察到的信号改变的细胞亚群的选择和生长。
我们观察到奥希替尼治疗HCC827-ER1的5例肿瘤组Met活化环Tyr1234的磷酸化水平升高。因此,考虑到这种异种移植模型的MET扩增,MET仍可能驱动许多对奥希替尼耐药的HCC827-ER1肿瘤的生长。JNJ-61186372可能有效地克服了这种耐药机制,因为在所有HCC827-ER1肿瘤中,使用该抗体治疗的肿瘤表现出MetTyr1234水平的显着降低。
总的来说,我们基于磷酸酪氨酸的蛋白质组方法揭示了耐药肿瘤细胞状态的多样性,并确定了独特的、异种移植物肿瘤特异性的、支持耐药生长的信号通路重组。
对奥希替尼和JNJ-61186372单药治疗的耐药性显示EGFR和SFK信号网络的下调
尽管持续使用EGFRTKI或基于抗体的EGFR和Met双重靶向治疗,仍出现耐药肿瘤的生长。因此,我们推测肿瘤以某种方式避开了EGFR/Met抑制以维持耐药生长。然而,来自含磷酪氨酸肽的磷酸化蛋白网络在大多数肿瘤中显示出明显的下降水平,证明EGFR和Met确实都受到抑制(除了对奥希替尼耐药的HCC827-ER1肿瘤中的Met)。重要的是,我们可以证实JNJ-61186372对EGFR信号通路的抑制作用,但在6小时的疗效分析中并不明显。而抑制表皮生长因子受体信号在H1975-HGF肿瘤耐JNJ61186372没有明显的字符串网络、表皮生长因子受体的比率此处则包含Tyr1092和Tyr1172网站显示平均比率为0.59±0.25,0.63±0.19,分别在肿瘤,从而显示出温和抑制。
与耐药肿瘤中被抑制的网络相反,上调的网络显示出少量的由线支撑的互联。然而,在几个耐药肿瘤组中,我们发现了p38MAPK(MAPK14)和pi3-激酶(PIK3R1或PIK3R2)的磷酸化,这表明一些常见的下游激酶可能在介导治疗反应或耐药中发挥中心作用。综上所述,这些发现表明耐药信号的上调更可能发生在单个肿瘤的基础上,而不是包含耐药肿瘤的共同特征。
沿着这些思路,我们分析了每个耐药肿瘤调控信号转导谱之间的激酶-底物关系。与我们的磷酸酪氨酸分析一致,我们发现EGFR、JAK2和Src激酶中激酶底物基序的表达有所增加。有趣的是,尽管我们的磷蛋白质网络分析显示抗肿瘤的主要趋势显示与伴随的Src家族激酶抑制EGFR抑制、表皮生长因子受体的浓缩,JAK2和Src激酶衬底图案让我们解读为每个单独的肿瘤一个独特和微分调节表皮生长因子受体,JAK2或Src基质。这一结果再次强调了个体耐药肿瘤的适应性反应存在明显的异质性。
考虑到EGFR和SFK信号之间良好的相互作用,我们推测SFK网络信号的减少可能与EGFR网络活性的降低有关。因为它已经建立,残留在表皮生长因子受体信号通路可以治疗抗表皮生长因子受体抑制剂,我们发现增加磷酸化SFK基质在某些个人的抗肿瘤,我们调查是否进一步抑制剩余剩余SFK活动可能增强细胞杀死奥希替尼的上下文中。
首先,在H1975-HGF和erlotinib耐药的HCC827细胞中,我们测定了奥希替尼和SFK抑制剂saracatinib和dasatinib的IC50值。用化合物确定的IC50值和奥希替尼与SFK抑制剂saracatinib或dasatinib的固定比值处理细胞,增强协同杀伤细胞。达沙替尼在erlotinib耐药的HCC827细胞中证实了这些结果。这些结果表明,尽管单独使用奥希替尼或JNJ-61186372治疗极大地抑制了EGFR和SFK信号,但残留的SFK信号可能足以促进肿瘤的持续生长或至少抑制肿瘤的生长。因此,通过结合EGFR和SFK抑制剂来消除残余的SFK活性,可能会显着延迟晚期NSCLC耐药的发生或潜在地消除耐药细胞的生长。奥希替尼哪里购买?仿制药比原研药便宜多少呢?详情请扫码咨询:










请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)